11/08/2012 09:52:28 AMPhương pháp kết tủa trong xử lý nước thải
(Lượt xem: 649)Cơ chế của quá trình này là việc thêm vào nước thải các hóa chất để làm kết tủa các chất hòa tan trong nước thải hoặc chất rắn lơ lửng sau đó loại bỏ chúng thông qua quá trình lắng cặn.
Trước đây người ta thường dùng quá trình này để khử bớt chất rắn lơ lửng, sau đó là BOD của nước thải khi có sự biến động lớn về SS, BOD của nước thải cần xử lý theo mùa vụ sản xuất; khi nước thải cần phải đạt đến một giá trị BOD, SS nào đó trước khi cho vào quá trình xử lý sinh học và trợ giúp cho các quá trình lắng trong các bể lắng sơ và thứ cấp. Các hóa chất thường sử dụng cho quá trình này được liệt kê trong bảng 6.1. Hiệu suất lắng phụ thuộc vào lượng hóa chất sử dụng và yêu cầu quản lý. Thông thường nếu tính toán tốt quá trình này có thể loại được 80 - 90% TSS, 40 - 70% BOD5, 30 - 60% COD và 80 - 90% vi khuẩn trong khi các quá trình lắng cơ học thông thường chỉ loại được 50 - 70% TSS, 30 - 40% chất hữu cơ.
Các hóa chất thường sử dụng trong quá trình kết tủa
|
Teân hoùa chaát
|
Coâng thöùc
|
Troïng löôïng phaân töû
|
Troïng löôïng rieâng, lb/ft3
|
|
Khoâ
|
Dung dòch
|
|
Pheøn nhoâm
|
Al2(SO4)3.18H2O
Al2(SO4)3.14H2O
|
666,7
594,3
|
60 ¸ 75
60 ¸ 75
|
78 ¸ 80 (49%)
83 ¸ 85 (49%)
|
|
Ferric chloride
|
FeCl3
|
162,1
|
|
84 ¸ 93
|
|
Ferric sulfate
|
Fe2(SO4)3
Fe2(SO4)3.3H2O
|
400
454
|
|
70 ¸ 72
|
|
Ferric sulfate (copperas)
|
FeSO4.7H2O
|
278,0
|
62 ¸ 66
|
|
|
Voâi
|
Ca(OH)2
|
56 theo CaO
|
35 ¸ 50
|
|
Nguồn: Wastewater Engineering: treatment, reuse, disposal, 1991
Ghi chú: lb/ft3 - 16,0185 = kg/m3
Sử dụng hóa chất để loại chất rắn lơ lửng
Phèn nhôm: khi được thêm vào nước thải có chứa calcium hay magnesium bicarbonate phản ứng xảy ra như sau:
Al2(SO4)3.18H2O + 3Ca(HCO)3 Û 3CaSO4 + 2Al(OH)3 + 6CO2 + 18H2O
Aluminum hydroxide không tan, lắng xuống với một vận tốc chậm kéo theo nó là các chất rắn lơ lửng. Trong phản ứng tên cần thiết phải có 4,5 mg/L alkalinity (tính theo CaCO3) để phản ứng hoàn toàn với 10 mg/L phèn nhôm. Do đó nếu cần thiết phải sử dụng thêm vôi để alkalinity thích hợp.
Vôi: khi cho vôi vào nước thải các phản ứng sau có thể xảy ra:
Ca(OH)2 + H2CO3 Û CaCO3 + 2H2O
Ca(OH)2 + Ca(HCO3)2 Û 2CaCO3 + 2H2O
Quá trình lắng của CaCO3 sẽ kéo theo các chất rắn lơ lửng.
Sulfate sắt và vôi: trong hầu hết các trường hợp sulfate sắt không sử dụng riêng lẻ mà phải kết hợp với vôi để tạo kết tủa. Các phản ứng xảy ra như sau:
FeSO4 + Ca(HCO3)2 Û 2Fe(HCO3)2 + CaSO4 + 2H2O
Fe(HCO3)2 + Ca(OH)2 Û 2Fe(OH)2 + 2CaCO3 + 2H2O
4Fe(OH)2 + O2 + 2H2OÞ 4Fe(OH)3
Khi Fe(OH)3 lắng xuống nó sẽ kéo theo các chất rắn lơ lửng. Trong các phản ứng này ta cần thêm 3,6 mg/L alkalinity, 4,0 mg/L vôi và 0,29 mg/L oxy.
Ferric chloride: phản ứng xảy ra như sau:
FeCl3 + 3 H2O Û Fe(OH)3 + 3H+ + 3Cl -
3H+ + 3HCO3 - Û 3H2CO3
Ferric chloride và vôi: phản ứng xảy ra như sau:
FeCl3 + Ca(OH)2 Û 3CaCl2 + 2Fe(OH)3
Ferric sulfate và vôi: phản ứng xảy ra như sau:
Fe2(SO4)3 + Ca(OH)2 Û 3CaSO4 + 2Fe(OH)3
Sử dụng hóa chất để loại bỏ phospho trong nước thải:
Vôi: như đã trình bày ở các phương trình trên, khi cho vôi vào nước thải nó sẽ phản ứng với bicarbonate alkalinity tạo thành kết tủa CaCO3. Trong môi trường pH > 10 các ion Ca+2 sẽ phản ứng với các ion PO4-3 tạo nên hydroxylapatite kết tủa. Để khỏi ảnh hưởng đến quá trình xử lý sinh học người ta thường dùng vôi ở liều lượng thấp 75 - 250 mg/L Ca(OH)2 và pH từ 8,5 - 9,5.
10 Ca+2 + 6 PO4-3 + 2 OH- Û 2Ca5(PO4)3OH
Phèn nhôm: phản ứng xảy ra như sau:
Al+3 + HnPO43-n Û AlPO4 + nH+
Các liều lượng phèn nhôm thường sử dụng và hiệu suất khử phospho của nó:
|
Hieäu suaát khöû phospho (%)
|
Tæ leä Mole (Al : P)
|
|
Khoaûng bieán thieân
|
Giaù trò thöôøng duøng
|
|
75
|
1,25 : 1 ¸ 1,5 : 1
|
1,4 : 1
|
|
85
|
1,6 : 1 ¸ 1,9 : 1
|
1,7 : 1
|
|
95
|
2,1 : 1 ¸ 2,6 : 1
|
2,3 : 1
|
Ferric: phản ứng xảy ra như sau:
Fe+3 + HnPO43-n Û FePO4 + nH+
Tùy theo bản chất của nước thải, qui trình xử lý mà giai đoạn khử phospho của nước thải có thề diễn ra ở bể lắng sơ cấp, bể lắng thứ cấp, bể lắng riêng đặt sau bể lắng thứ cấp. Hình 6.1 chỉ ra các sơ đồ của quá trình khử phospho bằng phương pháp hóa học.
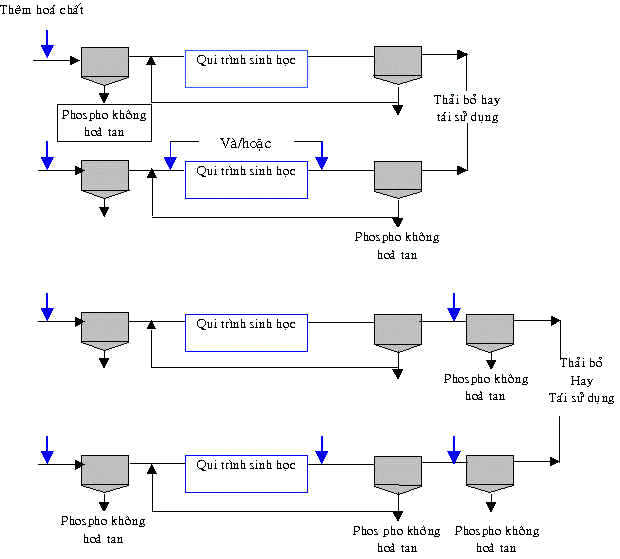
Sơ đồ của quy trình khử Photpho bằng phương pháp hóa học
Lưu lượng nạp nước thải cho bể lắng trong trường hợp có sử dụng hóa chát trợ lắng
|
Loaïi hoùa chaát
|
Löu löôïng naïp nöôùc thaûi gal/ft2.d
|
|
Khoaûng cho pheùp
|
Giaù trò thöôøng duøng
|
|
Phèn nhôm
|
600 ¸ 1200
|
1200
|
|
Ferric
|
600 ¸ 1200
|
1200
|
|
Vôi
|
750 ¸ 1500
|
1500
|
|
Nước thải không hóa chất
|
600 ¸ 1200
|
1200
|
Nguồn: Wastewater Engineering: treatment, reuse, disposal, 1991
Ghi chú: gal/ft2.d x 0,0407 = m3/m2.d
Kết tủa các kim loại nặng
Chuyển các chất thải dạng hòa tan sang dạng không hòa tan sau đó loại khỏi dung dịch bằng quá trình lắng, lọc.
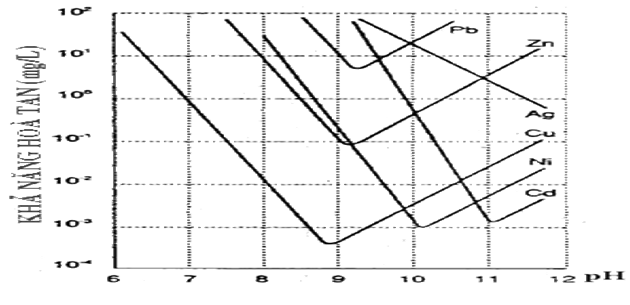
pH là một nhân tố quan trọng cho quá trình kết tủa. Bảng dưới đây đưa ra độ pH thích hợp cho quá trình kết tủa các kim loại nặng.
pH thích hợp cho việc kết tủa kim loại.
|
Ion
|
pH
|
Ion
|
pH
|
|
Fe (+3)
|
2,0
|
Ni (+2)
|
6,7
|
|
Al (+3)
|
4,1
|
Cd (+2)
|
6,7
|
|
Cr (+3)
|
5,3
|
Co (+2)
|
6,9
|
|
Cu (+2)
|
5,3
|
Zn (+2)
|
7,0
|
|
Fe (+2)
|
5,5
|
Mg (+2)
|
7,3
|
|
Pb (+2)
|
6,0
|
Mn (+2)
|
8,5
|
♣Tổng hợp bởi: www.vinaxanh.vn
♣Hãy thông tin cho chúng tôi để được hỗ trợ…!